Teilweise unseriöse Forschungsberichte
Vorwort
Sehr geehrte Leserinnen und Leser,
ein Begriff, der eigentlich aus der Wissenschaft kommt, der aber häufig auch außerhalb der wissenschaftlichen Forschung genutzt wird, ist der der klinischen Studie. Oftmals werden Produkte wie Körperpflegeprodukte, Cremes oder Nahrungsergänzungsmittel mit dem Prädikat „klinisch getestet“ beworben, ohne dass anhand des Produkts oder der Werbung deutlich werden müsste, was genau denn klinisch bedeutet. Auch die durchgeführten Tests sind oftmals sehr vielfältig und für den Laien ist es nur schwer nachzuvollziehen, wie der Hersteller des Produkts die Wirksamkeit bewiesen haben will. Im häufigsten Fall – um dies vorweg zu nehmen – bedeutet „klinisch getestet“ nicht mehr und nicht weniger, als dass das beworbene Produkt nicht schädlich ist. Wenn man betrachtet, was im Laufe der Geschichte alles genutzt wurde, um beispielsweise Haarausfall zu bekämpfen (siehe Artikel Mythen über Haarausfall), kann nicht schädlich durchaus als Vorteil verstanden werden, aber das heißt noch nicht, dass das Produkt auch einen positiven Effekt hat.
 Im Zusammenhang damit kommt es aus meiner Sicht nicht gerade selten dazu, dass das Prädikat „klinisch getestet“ besonders gern für Haarpflegeprodukte genutzt wird. Die Eigenschaft „klinisch getestet“ soll dann oftmals suggerieren, dass das Produkt positive Effekte auf die Haardichte oder die Haartextur hat oder vor Haarausfall schützt. Jedoch sollte solchen Versprechen mit Vorsicht begegnet werden, denn oftmals beweisen die Tests überhaupt nicht, was durch die Werbung suggeriert wird. Deshalb möchte ich die Gelegenheit nutzen und Ihnen im Rahmen dieses aktuellen Artikels darlegen, was klinische Studien eigentlich sind und durch welche Merkmale sie sich von der Art von Studien unterscheiden, die zu Werbezwecken als „klinisch“ bezeichnet werden. Auf diese Weise sollen Sie ein besseres Gefühl dafür bekommen, welchen Werbebotschaften Sie trauen können und welchen Sie besser argwöhnisch gegenüberstehen sollten.
Im Zusammenhang damit kommt es aus meiner Sicht nicht gerade selten dazu, dass das Prädikat „klinisch getestet“ besonders gern für Haarpflegeprodukte genutzt wird. Die Eigenschaft „klinisch getestet“ soll dann oftmals suggerieren, dass das Produkt positive Effekte auf die Haardichte oder die Haartextur hat oder vor Haarausfall schützt. Jedoch sollte solchen Versprechen mit Vorsicht begegnet werden, denn oftmals beweisen die Tests überhaupt nicht, was durch die Werbung suggeriert wird. Deshalb möchte ich die Gelegenheit nutzen und Ihnen im Rahmen dieses aktuellen Artikels darlegen, was klinische Studien eigentlich sind und durch welche Merkmale sie sich von der Art von Studien unterscheiden, die zu Werbezwecken als „klinisch“ bezeichnet werden. Auf diese Weise sollen Sie ein besseres Gefühl dafür bekommen, welchen Werbebotschaften Sie trauen können und welchen Sie besser argwöhnisch gegenüberstehen sollten.
In diesem Sinne wünsche ich Ihnen viel Freude bei der Lektüre!
Herzlichst
Ihre Angela Lehmann
Was sind klinische Studien und welche Merkmale unterscheiden sie von anderen Formen der Forschung?
Eine klinische Studie bezeichnet zunächst eine besondere Form der Datenerhebung oder allgemein der Untersuchung eines neu entwickelten Behandlungsverfahrens, wie beispielsweise eines Medikaments oder eines medizinischen Apparates. Allgemein lassen sich solche Studien anhand mehrerer Aspekte einteilen. Dabei kann zum einen grob zwischen Aspekten des Studiendesigns unterschieden werden, die die wissenschaftliche Aussagekraft der Studie beeinflussen. Zu diesen Aspekten zählen:
- Ist die Studie placebokontrolliert? Gab es also eine Versuchsgruppe, die eine Behandlung oder ein Medikament bekommen hat, das nachweislich keine Wirkung haben kann und wurde diese Gruppe mit denjenigen verglichen, die die eigentliche Behandlung oder das eigentliche Medikament tatsächlich bekamen?
- Handelt es sich um eine randomisierte Studie? Wird also zufällig festgelegt, wer in welcher Versuchsgruppe ist oder erfolgt die Zuteilung zur Behandlungs- beziehungsweise Placebogruppe auf Basis vorher festgelegter Kriterien?
- Wird die Studie einfach- oder doppelblind durchgeführt oder ist sie offen? Offen bedeutet, dass sowohl die Forscher als auch Teilnehmer der Studie wissen, ob sie in der Placebo- oder Behandlungsgruppe sind. Im Falle einer einfachen „Verblindung“ wissen es nur die Teilnehmer nicht und bei einer doppelblind geführten Studie ist zudem auch den Forschern nicht bekannt, ob der Proband, dessen Daten gerade ausgewertet werden, in der Behandlungs- oder Placebogruppe war
Gegebenenfalls können auch andere Aspekte des Studiendesigns unterschieden werden, aber mit den drei oben erläuterten sind die wichtigsten Aspekte vorerst zusammengefasst.
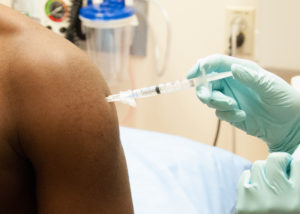
© NIAID | Teilnehmer einer medizinischen Studie wird ein Wirkstoff in den Arm injiziert.
© NIAID under
Creative Commons Attribution License
Weiterhin können klinische Studien nach ihrer Phase eingeteilt werden. Diese Phasen zerfallen zunächst in einen präklinischen und einen klinischen Abschnitt. Der präklinische Teil der Untersuchung dient der Grundlagenforschung zur mutmaßlichen Wirkungsweise des neuen Medikaments oder dem Vergleich verschiedener Wirkstoffkandidaten. Dabei spielen Modellsysteme, die einen verschiedenartigen Aussagewert der präklinischen Versuche haben, eine große Rolle. Hier kann zwischen in-vitro-Versuchen und in-vivo-Versuchen unterschieden werden. Bei den in-vitro-Versuchen wird der neue Wirkstoff beispielsweise von Bakterien hergestellt oder sein Einfluss auf die Stoffwechseldynamik von Hefezellen untersucht. Allen in-vitro-Versuchen ist gemein, dass sie im Reagenzglas (lateinisch: in vitro) durchgeführt werden. Demgegenüber wird der neue Wirkstoff bei in-vivo-Versuchen an Lebewesen getestet, um seine Wirkung auf einen komplexeren Organismus zu untersuchen. In beiden Fällen ist jedoch zu beachten, dass die Erkenntnis aus in-vitro- und in-vivo-Versuchen kaum bis gar nicht auf den Menschen übertragbar sein müssen. In dieser präklinischen Phase geht es, wie oben erwähnt, um Grundlagenforschung.
Verlaufen alle diese Versuche erfolgversprechend, kann die Behandlungsmethode oder das Medikament für eine klinische Überprüfung zugelassen werden. Diese gliedert sich weiterhin in vier Phasen, wobei manche Quellen auch eine Phase 0 erwähnen, auf deren Beschreibung an dieser Stelle allerdings verzichtet wird. In Phase I wird das Medikament zumeist jungen, gesunden, männlichen Erwachsenen verabreicht. Das hat den Hintergrund, dass zunächst die Sicherheit des Medikaments getestet werden soll. Im Falle weiblicher Probanden würde man beispielsweise eine Schädigung der Eizellen riskieren, wohingegen bei männlichen Probanden die Keimzellen beständig neu gebildet werden. Weiterhin sollten die Probanden in dieser Phase meist gesund sein, da sich sonst keine Schlüsse ziehen lassen, ob ein beobachteter Effekt auf der Krankheit oder dem Medikament basiert. Weiterhin wird in Phase I auch ermittelt, wie lange das Medikament im Körper bleibt, wie es metabolisiert wird und ob es Nebenwirkungen hat. In Phase-II-Studien wird das Medikament dann erstmals an Personen getestet, die an der Zielerkrankung leiden. Hier wird geprüft, ob das theoretische Therapiekonzept, was auf Basis der präklinischen Daten erstellt wurde, richtig ist (Phase IIa). Neben auftretenden Nebenwirkungen wird darüber hinaus auch versucht, die optimale Dosierung zu finden (Phase IIb). In den sogenannten Phase-III-Studien muss das Medikament unter Beweis stellen, dass es bei einer größeren Zahl erkrankter Probanden wirksam ist. Liegt ein signifikanter positiver Wirkungsnachweis für das Medikament vor (Phase IIIa), wird die Marktzulassung für das Präparat beantragt, was dann Phase IIIb entspricht. In der letzten Phase IV werden die zugelassenen Medikamente schließlich auf Wechselwirkungen mit anderen Präparaten hin untersucht beziehungsweise wird geprüft, ob die Einnahme sehr seltene (weniger als 1 von 10‘000) Nebenwirkungen zur Folge hat.
Diesem beschriebenen Vorgehen liegt eine engmaschige Kontrolle aller Ergebnisse durch unabhängige Stellen zugrunde. Die Durchführung derartiger klinischer Studien ist meist mit einem Aufwand von mehreren Millionen Dollar sowie mehreren Jahren der Entwicklung und Forschung verbunden. Die Zulassung der Präparate und Überwachung der Studien erfolgen in den USA durch die Food and Drug Administration, in der Europäischen Union durch die Kommission und die Mitgliedsstaaten und in der Schweiz durch Swissmedic mit Sitz in Bern.
Was sind Kriterien, anhand derer Sie die Qualität von klinischen Studien beurteilen können?
Nachfolgend gehen wir genauer auf einige Faktoren ein, anhand derer Sie die Qualität beziehungsweise Seriosität von klinischen Studien beurteilen können. Prinzipiell ist alles, was Sie hierfür benötigen, ein Internetzugang.
Wurde die Studie veröffentlicht und falls ja, wo?
Beim Prädikat „klinisch getestet“ und seinen Synonymen handelt es sich zunächst um eine nicht geregelte Werbeaussage, die für keinerlei Qualitätsprädikat steht. Jemand, der ein Produkt mit einer klinischen Testung bewirbt, wird jedoch auch irgendwie auf das Ergebnis der Testung verweisen. Beispielsweise wird in Fernsehwerbung für sogenannte Anti-Aging-Cremes häufiger erwähnt, dass ein großer Anteil der Anwenderinnen sehr zufrieden ist. Dementsprechend gehen beispielsweise einige Anbieter von Haarpflegeprodukten weiter und verweisen auf ihren Internetauftritten auf solche Studien. Als Qualitätsmerkmal gilt hierbei, dass die Studie von einem wissenschaftlichen Journal zur Publikation angenommen wurde. Dies kann zum Beispiel überprüft werden, indem der Studientitel in wissenschaftlichen Datenbanken gesucht wird. Finden sich dort die Angaben zum veröffentlichenden Journal, zur Ausgabe, in dem die Studie erschien und dem Veröffentlichungsjahr, kann davon ausgegangen werden, dass es sich tatsächlich um eine wissenschaftlich veröffentlichte Studie handelt. Demgegenüber darf jeder Hersteller im Rundfunk oder auf seiner Internetseite behaupten, dass sein Produkt klinisch getestet wurde. Wenn hierzu aber keine öffentlich zugänglichen Daten existieren, bleibt das lediglich eine Behauptung.
Zurück zum Inhaltsverzeichnis
Wie wurden die Erkenntnisse in der Studie gewonnen?
Dies ist ein sehr weites Feld, auf dem viele Faktoren zu beachten sind. Beispielsweise zählt dazu, ob die Studie mit Probanden durchgeführt wurde oder ob es sich lediglich um die oben beschriebenen in-vitro-Versuche handelt. Dieser Unterschied ist insofern wichtig, als dass auch in-vitro-Studien existieren, die zum Beispiel den Haarwuchs einzelner Kopfhautbiopsate untersuchen. Es mag vielleicht nicht weiter verwundern, dass das Haar weiterwächst, wenn man ein Stück Kopfhaut, in dem sich Haarfollikel befinden, in eine geeignete Nährlösung einlegt und dann den Haarwuchs misst; jedoch ist diese Versuchsanordnung hochgradig artifiziell und hat mit dem natürlichen Wachstum als Bestandteil eines Organismus nicht mehr viel zu tun. Dennoch lassen sich mit solchen Experimenten möglicherweise Resultate erzielen, die dem Produkt eine Wirkung bescheinigen, die es dann am ganzen Menschen gar nicht hat.

© INRA DIST under
Creative Commons Attribution 2.0 License
Etwas anders stellt sich der Sachverhalt dar, wenn eine Studie mit Probanden durchgeführt wurde. Zuerst ist dabei bedeutsam, wie die Teilnehmer rekrutiert wurden. Wurden sie zufällig ausgewählt und einer Behandlungs- oder Placebogruppe zugeteilt oder ist es vielmehr so, dass sie ein Leiden haben, dass sie möglicherweise durch die Teilnahme an der Studie beseitigen wollten? Hier spielt die Motivation der Teilnehmer eine nicht unerhebliche Rolle. Auch sollte darauf geachtet werden, ob sich bei den Teilnehmern eine besonders große Altersspanne zeigt. Wenn das so ist, leiden die Teilnehmer möglicherweise auch unter anderen Erkrankungen, die einen Einfluss auf die Tests haben können. Sind solche Erkrankungen angegeben oder wird einfach auf die Nennung verzichtet?
Weiterhin sollte beachtet werden, wie viele Personen an der Untersuchung teilgenommen haben. Da wissenschaftliche Untersuchungen in der Regel sehr teuer sind, können es nicht beliebig viele sein. Jedoch dürfen es andererseits auch nicht zu wenige sein, da die Untersuchung sonst kaum einen Aussagewert hat. Der Idealfall sieht so aus, dass die Untersucher eine Berechnung durchgeführt haben, wie viele Probanden sie untersuchen müssten, um einen Effekt nachweisen zu können.
Einer der wichtigsten Punkte bezieht sich auf die Versuchsführung selbst und meint die Objektivität oder Subjektivität eines Versuchsdesigns. Gerade bei Studien zu nicht medizinischen Pflegeprodukten werden den Teilnehmern oftmals Selbsteinschätzungsfragebögen zur Beantwortung vorgelegt. Dabei dürfte es für die meisten Menschen schwer sein, die dort abgefragten Aspekte auf wissenschaftlichem Niveau einzuschätzen. Beispielsweise wird dort nach dem Eindruck der Probanden gefragt, nach dem Auftragen einer Creme mehr oder weniger Fältchen zu haben. Ihre Antwort dürfte im wissenschaftlichen Sinne keine Aussagekraft haben. Insbesondere wenn die Probanden schon zu Studienbeginn vermehrt Fältchen hatten, und möglicherweise darunter litten, wird das Bild, das einer solchen Selbsteinschätzung zugrunde liegt, so stark verzerrt, dass daraus keine stichhaltigen Informationen mehr ableitbar sind. Um diesen Umstand abzumildern, werden auch häufiger Mediziner, die solche Untersuchungen begleiten, nach ihrem ärztlichen Eindruck gefragt. Dieser sollte zwar weniger verzerrt sein, aber ein objektivierbares Messergebnis liefert auch er nicht.
Werden Nebeneffekte berichtet oder wird Auskunft zur Handhabbarkeit gegeben?
Jede Untersuchung, die einen wissenschaftlichen Anspruch erheben will, muss konsequent über unerwartete Nebeneffekte und -wirkungen berichten, die im Rahmen der Untersuchung bei den Probanden auftraten. Im besten Fall sind solche Effekte nicht aufgetreten. Doch selbst das müsste irgendwo vermerkt werden. Dann kann der Leser für sich daraus schließen, dass mit der Anwendung des Produkts wenigstens keine bekannten negativen Folgen verknüpft sind. Seine Anwendung ist dementsprechend nicht schädlich, was aber keine Aussage über die Wirkung zulässt, denn die Wirksamkeit oder Unwirksamkeit einer medizinischen Behandlung korreliert nicht zwangsläufig mit den Nebenwirkungen, die sie haben kann.
Weiterhin sollte der Leser einer solchen Studie prüfen, ob die Anwendung, so wie sie im Rahmen der Untersuchung durchgeführt wurde, überhaupt praktikabel ist. Das meint zum einen, dass die Versuchsbedingungen möglichst „physiologischen“ Umständen entsprechen. Dieses Kriterium würde beispielsweise nicht erfüllt, wenn der Wirkstoff eines Nahrungsergänzungsmittels nur in so hohen Konzentrationen einen Effekt erzielt, dass dies die Einnahme von mehreren Kilogramm des Präparates an einem Tag erfordern würde. Ein anderes Beispiel wäre eine Substanz gegen Haarverlust (Alopezie), die über mehrere Stunden in Kontakt mit der Kopfhaut bleiben muss, um zu wirken. Dies wäre ein Zeitraum, der weit über die normale Dauer einer Haarwäsche hinausgeht. Zum anderen sollte sich jeder künftige Anwender solcher Präparate überlegen, ob die Anwendung überhaupt mit seinem Lebensstil und seinen Verhältnissen vereinbar ist. Das meint die Überlegung, ob die Kosten für die kontinuierliche Anwendung einer Hautcreme zur Faltenbekämpfung langfristig tragbar sind; oder auch, ob es die Nutzung eines Shampoos gegen Haarausfall erforderlich macht, die bisherigen Haarwaschgewohnheiten grundlegend zu ändern.
Werden aus den Studienergebnissen möglicherweise unzulässige Verallgemeinerungen geschlussfolgert?
Oftmals kommt es vor – und das betrifft zweifellos nicht nur „klinische Studien“ –, dass die Autoren wissenschaftlicher Veröffentlichungen unzulässige Verallgemeinerungen aus den Ergebnissen ableiten. Damit soll niemandem unterstellt werden, dies in vorsätzlicher oder gar böswilliger Art und Weise zu tun. Es genügt schon, sich über Jahre hinweg wissenschaftlich sehr intensiv mit einem Forschungsbereich auseinanderzusetzen, um schnell den Blick dafür zu verlieren, an welcher Stelle eine kausale Schlussfolgerung sinnvoll zu ziehen ist. Um dies deutlich zu machen, soll ein Analogiebeispiel herangezogen werden.
Der Hersteller von Mitteln (Medikamente, Lotionen, Shampoos oder Geräten), die Haarausfall verhindern sollen, testet sein Produkt und stellt bei der Messung fest, dass sich die Geschwindigkeit des Haarwachstums erhöht, wenn das Präparat eingenommen wird. Anschließend wird der potenziellen Kundschaft in Form der Werbeaussage suggeriert, dass das klinisch getestete Präparat das Haarwachstum anregt. Die Aussage ist dahingehend richtig, dass das Mittel tatsächlich bewirkt, dass vorhandenes Haar schneller wächst. Was die Werbebotschaft jedoch in diesem Sinne verschweigt, ist, dass diese nur auf noch gesunde Haarfollikel zutrifft. Bereits abgestorbene Follikel können nicht „wiederbelebt“ werden. Dies zu erkennen, ist aber lediglich möglich, wenn die zugehörige Publikation betrachtet wird.
Gibt es methodische oder finanzielle Unklarheiten bezüglich der veröffentlichten Daten?
Ein letzter Punkt, an dem sich leicht erkennen lässt, ob eine durchgeführte Studie als seriös zu beurteilen ist, betrifft potenzielle methodische oder finanzielle Verstrickungen. Um diese nachzuweisen oder auch nur erkennen zu können, sind aber oftmals umfangreichere Recherchen nötig.
Methodisch wird es beispielsweise dann schwierig, wenn der Untersucher einer Fragestellung das Untersuchungsverfahren entwickelt hat. Dieser Punkt mag zunächst nicht argwöhnisch erscheinen, jedoch ist es oftmals so, dass in Fachpublikationen nicht alle Einzelheiten eines Versuchs angegeben sind. Damit ist eine Detailtreue gemeint, die es jedem Leser mit dem Zugang zu den entsprechenden Untersuchungsgeräten oder Chemikalien ermöglichen würde, die Experimente selbst durchzuführen. Wesentlich häufiger als eine solch detaillierte Methodenbeschreibung findet sich aber der Verweis auf frühere Publikationen in der Form: „Der genaue Versuchsablauf wurde früher genau beschrieben (QUELLE).“ Widmet sich der Leser nun der Lektüre dieser neuen Quelle, kann er mitunter feststellen, dass sowohl die Untersuchungsmethodik als auch die mit dieser Methodik gewonnenen Resultate von ein und derselben Person stammen. Abhängig von der Prüfung des Einzelfalls kann dies die Aussagekraft der veröffentlichten Daten einschränken. Auch dies gilt, ohne den Untersuchern dabei anrüchige Motive unterstellen zu wollen.
Noch fragwürdiger stellt sich eine Studie möglicherweise beim Lesen des sogenannten Interessenkonfliktes (Conflict of Interest) dar. Dies ist ein spezieller Abschnitt einer wissenschaftlichen Publikation, in dem die Forscher angeben müssen, ob irgendwelche finanziellen oder beruflichen Interessen die Anfertigung der Publikation beeinträchtigt haben oder ob irgendwie geartete Interessen von Dritten durch die Veröffentlichung der Daten tangiert werden. Ist das der Fall, sind die Autoren der Studie dazu aufgefordert, diese im Abschnitt Interessenkonflikt offenzulegen. Gleichzeitig finden sich im Interessenkonflikt manchmal brisante Inhalte. Dies kann beispielsweise der Fall sein, wenn dort erklärt wird, dass sowohl die Studie von einem Unternehmen finanziert wurde und die Forscher gleichzeitig auch finanzielle Zuwendungen von demselben Unternehmen erhalten haben. Noch schwieriger stellt sich die Sache dar, wenn das besagte Unternehmen auch der Hersteller des Medikaments oder Gerätes ist, das dort auf seine Wirksamkeit hin getestet wird. Solche Konstellationen sind keinesfalls ungewöhnlich und in vielen Fällen auch unproblematisch, denn es mag nicht verwundern, dass viele Unternehmen auf der Welt ein Interesse daran haben, dass die Wirksamkeit ihrer Produkte wissenschaftlich bewiesen wird. Es sei auch darauf hingewiesen, dass solche Angaben oder solche Beziehungskonstellationen zwischen Forschern und Unternehmen nicht illegal sind. Maximal sind sie ethisch fragwürdig. Dies sollte jedoch keinesfalls darüber hinwegtäuschen, dass ein aufmerksamer Leser solche Geschäftsbeziehungen hinreichend in seine Überlegungen einfließen lässt, ob ein nichtmedizinisches Produkt noch als „klinisch getestet“ gelten soll.
Sind Sie sich noch immer unschlüssig, ob eine Publikation seriös ist?
Wenn eine Publikation die bisher in diesem Artikel diskutierten Qualitätsanforderungen erfüllt, können Sie schon mit großer Sicherheit davon ausgehen, dass es sich um eine seriöse Veröffentlichung handelt. Falls Sie jedoch immer noch Zweifel daran haben, wie Daten zustande gekommen sind, folgt hier ein letzter Tipp für Sie:
Neben den Unternehmen, die die Durchführung wissenschaftlicher Studien fördern können, gibt es in nahezu jedem Land der Welt, das sich wissenschaftlich engagiert, eine entsprechende Kontrollbehörde für die Vergabe von Forschungsgeldern. Bei der Antragstellung wird von vielen dieser Institutionen gefordert, dass ein sogenanntes Datenmanagement entwickelt wird. Dies zielt darauf ab, die ursprünglichen Primärdaten aus den Experimenten so vielen anderen Forschern und Prüfern zugänglich zu machen, damit sie überprüft und validiert werden können. Fragen Sie gegebenenfalls an, ob Sie Zugriff auf die Rohdaten erhalten können; dann können Sie selbst nachrechnen, ob aus dem, was in den Experimenten berechnet wurde, die richtigen Schlüsse gezogen werden. Andernfalls haben Sie auch die Möglichkeit die Forscher selbst zu fragen; denn schließlich steht auf jeder Publikation eine Referenzadresse, unter der publizierende Forscher erreichbar sein sollten. Manchmal lohnt es sich nachzufragen und ein zweites Mal hinzuschauen!

